僧帽弁閉鎖不全症とは
僧帽弁閉鎖不全症(Myxomatous Mitral Valve Disease: MMVD)は、特に小型犬に非常に多く見られる後天性の心臓病です 。僧帽弁(左心房と左心室の間にある弁)とその支持組織(腱索など)が粘液腫様変性という変化を起こし、弁がうまく閉じなくなることで血液の逆流が生じます 。
キャバリア・キング・チャールズ・スパニエル、ミニチュア・ダックスフンド、トイ・プードル、チワワなどで好発します 。
病気の進行は個体差がありますが、多くは無症状の期間を経て徐々に進行し、心拡大、そして最終的には肺うっ血(肺水腫)や低心拍出量による臨床症状(咳、呼吸困難、失神など)を引き起こす「うっ血性心不全(CHF)」に至ります 。
アニマルドックや春・秋の健康診断コースで早期発見できる場合があります。
目次
米国獣医内科学会(ACVIM)のガイドラインを中心に、各ステージの診断と治療について解説します 。
MMVDのリスクは高いが、心臓の構造的異常はない段階 。
僧帽弁閉鎖不全症(MMVD)を発症するリスクが高く、現時点で心臓の構造的異常(心雑音など)がなくてもステージAに分類される犬種として、以下の犬種が挙げられています。
キャバリア・キング・チャールズ・スパニエル
ダックスフンド(特にミニチュア・ダックスフンド)
トイ・プードル
ミニチュア・プードル
チワワ (日本で特に多いとされています)
薬物療法や食事療法は不要 。早期に診断された繁殖犬は繁殖中止 。
これらの犬種や、その他MMVDを発症しやすいとされる小型犬種 は、症状や心雑音がなくても定期的な健康診断(年1回の聴診など) を受けることが推奨されています。
心拡大が認められないか、軽微な段階 。心不全症状はない 。
胸部レントゲン、血圧測定、心エコー検査が推奨 。
薬物療法や食事療法は不要 。6〜12ヶ月ごとの再検査 。
明らかな心拡大(左房・左室拡大)があり、心不全発症リスクが高い段階 。
心雑音グレード3/6以上 、心エコー(LA/Ao比≧1.6, LVIDDN≧1.7 )、レントゲン(VHS>10.5 )を満たす場合。
心エコー所見が最も信頼性が高いとされます 。レントゲンのみの場合はVHS≧11.5やVLAS≧3などが参考になります 。
診断基準について
まだ元気で症状(咳や息切れなど)が出ていなくても、心臓の中では病気が少しずつ進行していることがあります。
「ステージB2」というのは、心臓弁の逆流によって心臓に負担がかかり、心臓が少し大きくなり始めた状態を指します。
この段階で治療を始めると、将来的に心不全の症状が出るのを遅らせることができるため、獣医師はこの基準を使って治療を開始すべきか判断します。
その基準となる検査結果は主に以下の3つです。
心臓弁がうまく閉じずに血液が逆流すると、「ザーザー」というような雑音が聴診器で聞こえます。
この雑音の大きさは6段階で評価され、「グレード3/6以上」というのは、中程度以上の比較的はっきり聞こえる雑音があることを意味し、弁の逆流がある程度進んでいるサインです。
これは心臓の動きや大きさを詳しく見るための、最も信頼性の高い検査です。
・LA/Ao比 ≧ 1.6: 左心房(血液が戻ってくる部屋)が、大動脈(全身に血液を送る太い血管)と比べて1.6倍以上に大きくなっていることを示します。
逆流した血液を受け止めるために、左心房がふくらんできている状態です。
・LVIDDN ≧ 1.7: 左心室(血液を力強く送り出すメインの部屋)が、ワンちゃんの体の大きさに対して基準値(1.7)以上に大きくなっていることを示します。
余分な血液を処理するために、左心室も大きくなってきている状態です。
心臓全体の形や大きさ、肺の状態を確認します。
VHS > 10.5: これは、背骨の長さと比べて心臓がどれくらい大きいかを測る数値です。10.5を超えていると、一般的に心臓が大きくなっていると考えられます。
もし心エコー検査が難しい場合、レントゲンだけでも心臓の大きさを評価します。その場合、VHSが11.5以上、あるいはVLAS(レントゲンでの左心房の大きさの指標)が3以上といった、よりはっきりとした拡大を示す数値を参考にすることがあります。
これらの検査結果を総合的に見て、ワンちゃんの心臓がステージB2の基準を満たしていると判断された場合、多くは心臓の負担を減らし、心不全の発症を遅らせるためのお薬(ピモベンダンなど)を開始することが推奨されます。
ピモベンダン: (0.25−0.3mg/kg 1日2回経口投与) 心不全発症を遅らせるため、強く推奨されます(クラスI、エビデンスA) 。
食事療法: 軽度のナトリウム制限、適切なタンパク質・カロリー摂取が推奨されます(クラスIIa、エビデンスC) 。
ACE阻害薬: 有効性については議論があり、ACVIMでは必須とはされていませんが 、推奨する専門家もいます(クラスIIa、エビデンスC) 。咳のコントロールに難渋する場合に試されることもあります 。
スピロノラクトン、β遮断薬: 通常推奨されません(クラスIII、エビデンスC/D) 。
咳: 心拡大による気道圧迫が原因の場合、鎮咳薬が考慮されることがあります(クラスIIa、エビデンスD) 。気管支拡張薬(テオフィリンなど)や、炎症が関与する場合は一時的なステロイドが有効なこともあります 。
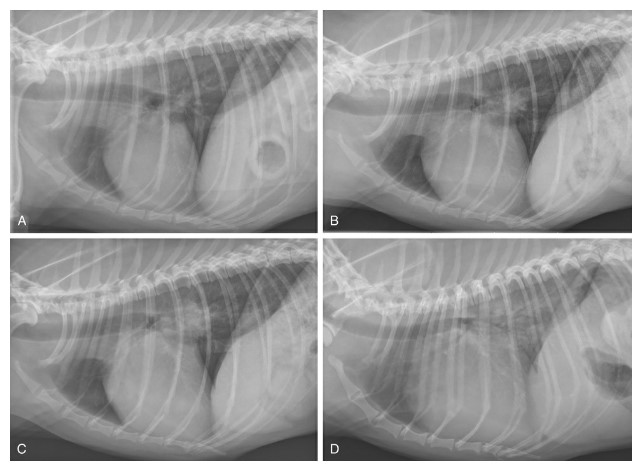
Ettinger’s Textbook of Veterinary Internal Medicineより引用
図232.2
僧帽弁粘液腫様変性(MMVD)がうっ血性心不全(CHF)に進行するにつれて起こる、心臓の大きさ、肺野、血管系の変化を示す左側胸部X線。
A:正常な心臓の輪郭と大きさ(椎骨心臓スコア[VHS] 10.2)、および著変のない肺野と血管系(ステージB1)。
B:軽度の心拡大(VHS 11.4)と正常な肺野および血管系(ステージB2初期)。
C:より進行した心拡大(VHS 12.2)で、気管の挙上とより顕著な血管像を伴うが、肺水腫の兆候はない(ステージB2後期)。
D:重度の心拡大(VHS 14.6)、および肺うっ血と間質性水腫(ステージC)。
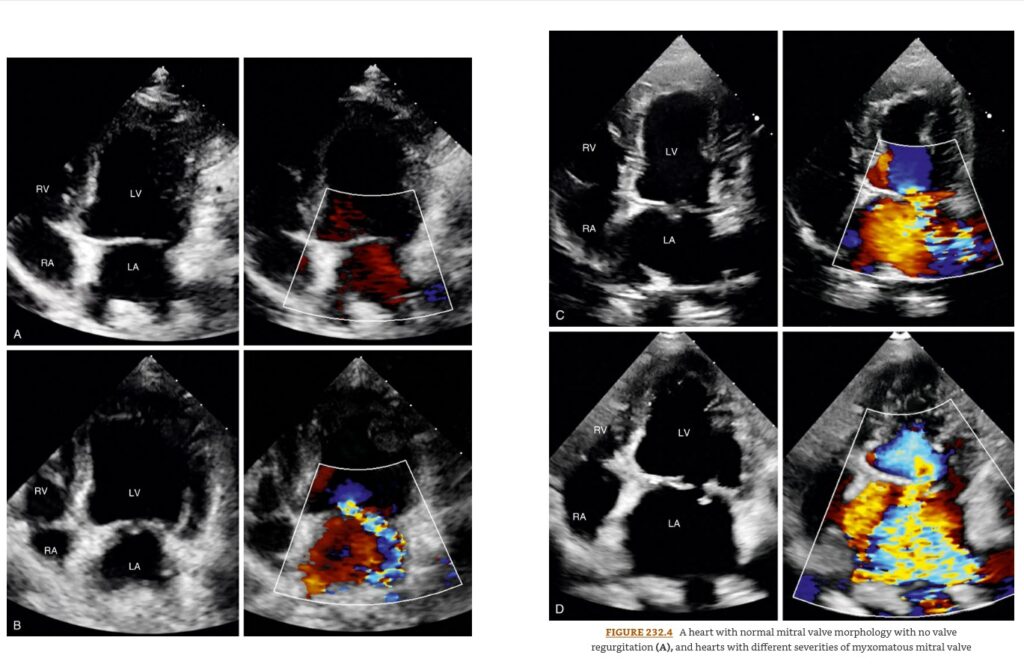
心不全症状(肺水腫など)を現在示している、または過去に示した段階 。
臨床症状、身体検査(心雑音、肺のクラックル音など)、レントゲン(心拡大、肺水腫像)、心エコー(心拡大、左房圧上昇所見 E波>1.2-1.4m/sなど)、血液検査(腎機能、電解質、NT-proBNPなど) を組み合わせて行います。
酸素吸入: 低酸素血症の改善 。
フロセミド: (1−2mg/kg 静注/筋注、反応を見ながら1時間ごとに追加、最大8mg/kg/4時間まで、あるいは0.66−1mg/kg/時で持続点滴も可)肺水腫の軽減 。
ピモベンダン: (0.25−0.3mg/kg 1日2回経口投与) 強心作用と血管拡張作用 。
血管拡張薬: ニトログリセリン軟膏(推奨度は低い クラスIIb) や、重症例ではニトロプルシド持続点滴 。血圧が高い場合(収縮期120mmHg以上など)はカルペリチド(ANP製剤、0.05-0.2 μg/kg/分を持続点滴)も有効な選択肢です 。
鎮静剤: 呼吸困難に伴う不安の軽減(ブトルファノールなど)。
穿刺: 胸水・腹水があれば排液 。
ACE阻害薬: 急性期での使用は議論あり(クラスIIb)。
標準治療として以下の4剤が基本となります(クラスI)。
フロセミド: (通常 1−2mg/kg 1日2回経口投与から開始し、症状や腎機能を見ながら最小有効量に調整)。安静時呼吸数をモニタリングし、再発の早期発見に努めます 。
ピモベンダン: (0.25−0.3mg/kg 1日2回経口投与) 。
ACE阻害薬: (例: エナラプリル、ベナゼプリル 0.5mg/kg 1日1-2回経口投与) 。
スピロノラクトン: (1−2mg/kg 1日1-2回経口投与) アルドステロン拮抗作用による心保護効果も期待されます 。
食事療法: ステージB2と同様ですが、心臓悪液質に注意し、十分なカロリーとタンパク質を確保します 。ナトリウム制限は継続します 。低カリウム血症が見られる場合はカリウム補給を検討します 。オメガ3脂肪酸の補給も考慮されます 。
トラセミド: フロセミドで効果不十分、あるいは副作用(腎機能悪化など)が懸念される場合に代替薬として考慮されます 。フロセミドの約1/10~1/20の用量 (0.1−0.3mg/kg 1日1回) が目安ですが、個体差が大きいです 。フロセミドより作用時間が長く、抗アルドステロン作用も併せ持ちます 。
標準治療に反応しない末期の心不全 。
ステージCの診断基準に加え、標準治療(フロセミド8mg/kg/日以上など)への抵抗性を確認 。
ステージCの治療を強化します。
利尿薬の調整: 腎機能が許容範囲であればフロセミドまたはトラセミドを増量します 。
フロセミド頻回投与(1日3回)、皮下投与なども考慮されます 。利尿薬抵抗性(RAAS活性化、腎血行動態変化、下位尿細管でのNa再吸収亢進など)が見られる場合は、作用機序の異なる利尿薬(ヒドロクロロサイアザイドなどサイアザイド系利尿薬)の併用が有効な場合があります 。ただし、腎機能障害や電解質異常のリスクが高まるため慎重なモニタリングが必要です 。
ピモベンダン増量: 1日3回投与(適用外使用)が考慮されることがあります 。
追加の血管拡張薬: アムロジピンやヒドララジンを追加し、後負荷をさらに軽減します 。
肺高血圧症: 合併している場合はシルデナフィル (1−2mg/kg 1日3回) を使用します 。
ジゴキシン: 心房細動のレートコントロール目的 、あるいは洞調律でも推奨する専門家もいます 。
β遮断薬: 通常は開始しませんが、心房細動コントロールや、以前から使用している場合は慎重に継続または減量を検討します 。
対症療法: 難治性の咳に対する鎮咳薬 や気管支拡張薬 。
バソプレシンV2受容体拮抗薬(トルバプタンなど): 水のみを排泄させる新しいタイプの利尿薬で、電解質異常を起こしにくい特徴があります 。今後の獣医療での応用が期待されます。
僧帽弁形成術(MVP)は、人工心肺を使用し、損傷した弁を修復する根治的な治療法です 。主に腱索再建(人工腱索を使用)と弁輪縫縮術が行われます 。
ACVIMステージB2後期、C、Dが主な対象です 。ステージDでも内科治療が限界であれば積極的に考慮されます 。他の疾患(腎臓病、肺高血圧症など)が併存する場合でも、MMVDが最も予後に影響すると判断されれば適応となることが多いですが、手術リスクは上昇する可能性があります 。
高度医療施設での実施が必要で、合併症のリスク(血栓、感染、腎障害など)も伴いますが、専門施設での成功率は高く(3ヶ月生存率96%以上など)、成功すれば多くの場合で心臓薬の投与が不要となり、年単位での予後延長が期待できます 。
まれに逆流の再発(変性の進行、人工腱索の問題など)や僧帽弁狭窄、三尖弁逆流の悪化などが起こる可能性があります 。
開心術を行わず、カテーテルを用いて僧帽弁の前尖と後尖をクリップで留置し、逆流を軽減する低侵襲治療法です 。人ではMitraClipが用いられますが、犬用にはV-Clampなどのデバイスが開発され、臨床応用が始まっています 。開心術のリスクが高い高齢や併発疾患を持つ症例に対する選択肢として期待されています 。
心不全を発症する前の段階であり、多くの場合、進行は緩やかです。すぐに心不全に至る可能性は低いですが、定期的な検査で進行を監視することが重要です。
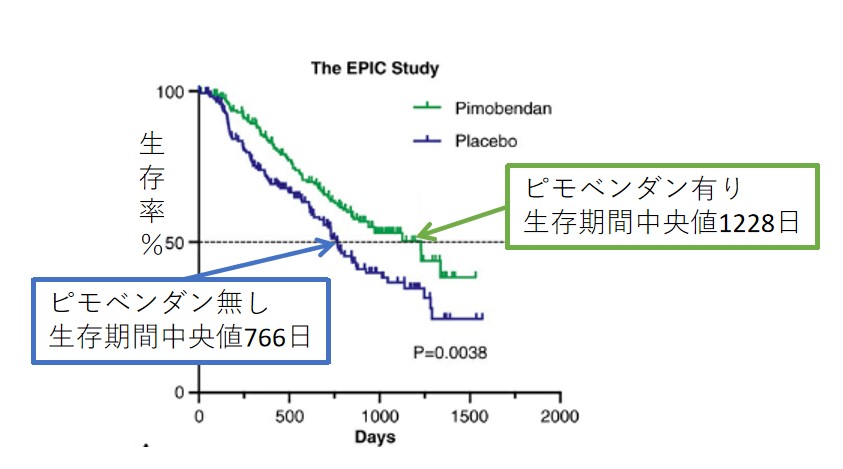
心拡大が始まっている段階ですが、臨床症状はありません。ピモベンダンによる治療を開始することで、心不全の発症を平均約15ヶ月遅らせることができると報告されています(EPICスタディ)。
このステージの犬は、心不全を発症するまで3〜4年以上生存することも少なくありません。ただし、左心拡大の程度やE波速度の上昇などが予後不良因子として知られています。
心不全を発症した段階です。適切な内科療法(利尿薬、ピモベンダン、ACE阻害薬、スピロノラクトンなど)により、症状を管理し生活の質(QOL)を維持することを目指します。ステージCおよびDの内科療法における生存期間の中央値(半数の犬が生存する期間)は、報告によって差がありますが、半年〜1年程度とされています。ただし、これは安楽死を選択された症例も含む場合があり、個々の状況によって大きく異なります。ステージDは治療抵抗性であり、予後はより厳しいです。
僧帽弁形成術は根治的な治療法であり、成功すれば内科療法と比較して大幅な予後の改善が期待できます。
手術が成功し、周術期(手術前後)を乗り越えることができれば、多くの場合、心臓薬の投与が不要または大幅に減量でき、年単位での生存期間の延長が期待されます。
ただし、手術にはリスクが伴い、合併症(血栓症、感染症、腎機能障害など)が起こる可能性もあります。手術成績は施設やチームの経験によって異なりますが、専門施設では高い成功率が報告されています。
ステージDのような末期的な症例でも手術は可能ですが、ステージB2やCと比較して周術期死亡率が高く、生存期間も短くなる傾向が報告されています。それでも内科治療が限界な場合には、手術が有力な選択肢となり得ます。
術後長期的に、まれに逆流の再発、僧帽弁狭窄、三尖弁逆流の悪化などが問題となる可能性もあります。
当然ながら、ステージが進行するほど予後は厳しくなります。
左心房・左心室の拡大が重度であるほど、予後は悪化する傾向があります。
E波速度の上昇などは、左房圧の上昇を示唆し、予後不良と関連します。
NT-proBNPなどの値が高い場合、予後が悪い傾向があります。
安静時心拍数が高いことも予後不良因子とされています。
腎臓病、肺高血圧症、不整脈などの併存疾患があると、予後に影響を与える可能性があります。
治療によく反応し、症状が安定している場合は、予後が良い傾向があります。
個々の犬の予後については、状態を詳しく評価した上で、かかりつけの獣医師や循環器専門医にご相談ください。
犬の僧帽弁閉鎖不全症は、ACVIMガイドラインに基づいたステージ分類に応じた内科的管理が基本となります。
近年ではピモベンダンの早期(ステージB2)導入が標準的となり、心不全ステージ(C、D)では利尿薬、ACE阻害薬、スピロノラクトンなどを組み合わせた多剤併用療法が行われます。
利尿薬の選択や調整には、効果と副作用(特に腎機能や電解質)のバランスを考慮した慎重な判断が必要です。
外科療法(僧帽弁形成術)は根治的な治療法として確立されつつあり、特定の施設で実施されています。低侵襲なカテーテル治療(TEER)も登場し、治療選択肢は広がりつつあります。
いずれの治療法を選択するにしても、個々の症例の状態を正確に評価し、飼い主と十分に相談した上で、最適な治療計画を立てることが重要です。
僧房弁閉鎖不全症はアニマルドックや春・秋の健康診断コースで早期発見できる場合があります。
 健康診断・アニマルドック
健康診断・アニマルドック  甲賀セレネ動物病院
甲賀セレネ動物病院

